Detección molecular de Rickettsia typhi en perros de una comunidad rural de Yucatán, México
Resumen
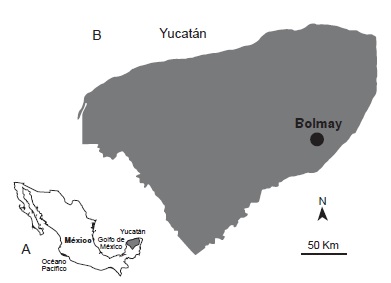
Introducción. Rickettsia typhi es la bacteria causante del tifus múrido o endémico, el cual es transmitido al ser humano principalmente por medio de las heces infectadas de pulgas y en cuyo ciclo de infección se encuentran involucrados distintos animales sinantrópicos y domésticos. En la comunidad rural de Bolmay, Yucatán, México, se reportaron casos de tifus múrido en seres humanos durante el periodo 2007-2010.
Objetivo. Identificar la presencia de R. typhi y estimar la frecuencia de infección en perros de Bolmay, México.
Materiales y métodos. Se tomaron muestras de sangre completa de 128 perros, se les extrajo el ADN total y se analizaron mediante reacción en cadena de la polimerasa (PCR) para amplificar los fragmentos del gen de 17 kDa y omp B, y confirmar la presencia de Rickettsia spp. Los productos de las reacciones se enviaron a secuenciación y se les hizo un análisis de alineamiento con Basic Local Alignment Search Tool (BLAST).
Resultados. Se encontró una frecuencia de infección de 5,5 % (7/128). El alineamiento demostró 99 % de homologación para el gen de 17 kDa y 100 % para el gen omp B en R. typhi.
Conclusión. Se detectó la presencia de R. typhi pero una baja frecuencia de infección en perros de la comunidad de estudio; sin embargo, la especie podría representar un riesgo de transmisión para los seres humanos.
Descargas
Referencias bibliográficas
Raoult D, Roux V. Rickettsioses as paradigms of new or emerging infectious diseases. Clin Microbiol Rev. 1997;10:694-719.
Milagres BS, Padilha AF, Padilha AF, Montandon CE, Freitas RN, Pacheco R, et al. Spotted fever group rickettsia in small rodents from areas of low endemicity for Brazilian spotted fever in the eastern region of Minas Gerais State, Brazil. Am J Trop Med Hyg. 2013;88:937-9. http://dx.doi.org/10.4269/ajtmh.12-0609.
Raoult D, Woodward T, Dumler JS. The history of epidemic typhus. Infec Dis Clin North Am. 2004;18:127-40. http://dx.doi.org/10.1016/S0891-5520(03)00093-X.
Parola P, Paddock CD, Raoult D. Tick-borne rickettsioses around the world: Emerging diseases challenging old concepts. Clin Microbiol Rev. 2005;18:719-56. http://dx.doi.org/10.1128/CMR.18.4.719-756.2005.
Wall R. A Ticking clock for tickborne disease? Vet Rec. 2012;170:326-8. http://dx.doi.org/10.1136/vr.e2158.
Rovery C, Brouqui P, Raoult D. Questions on Mediterranean spotted fever a century after its discovery. Emerg Infect Dis. 2008;14:1360-7. http://dx.doi.org/10.3201/eid1409.071133.
Nogueras MM, Pons I, Pla J, Ortuño A, Miret J, Sanfeliu I, et al. The role of dogs in the eco-epidemiology of Rickettsia typhi, etiological agent of murine typhus. Vet Microbiol. 2013;163:97-102. http://dx.doi.org/10.1016/j.vetmic.2012.11.043.
Breitschwerdt EB, Meuten DJ, Walker DH, Levy M, Kennedy K, King M, et al. Canine Rocky Mountain spotted fever: A kennel epizootic. Am J Vet Res. 1985;46:2124-8.
Nicholson WL, Allen KE, McQuiston JH, Breitschwerdt EB, Little SE. The increasing recognition of rickettsial pathogens in dogs and people. Trends Parasitol. 2010;26: 205-212. http://dx.doi.org/10.1016/j.pt.2010.01.007.
Adjemian J, Parks S, McElroy K, Campbell J, Eremeeva ME, Nicholson WL, et al. Murine typhus in Austin, Texas, USA, 2008. Emerg Infect Dis. 2010;16:412-7. http://dx.doi.org/10.3201/eid1603.091028.
Zavala-Castro JE, Zavala-Velázquez JE, Sulú-Uicab JE. Murine typhus in child, Yucatán, México. Emerg Infect Dis. 2009;15:972-4. http://dx.doi.org/10.3201/eid1506.081367.
Dzul-Rosado K, González-Martínez P, Peniche-Lara G, Zavala-Velázquez J, Zavala-Castro J. Murine typhus in humans, Yucatan, Mexico. Emerg Infect Dis. 2013;19: 1021-2. http://dx.doi.org/10.3201/eid1906.121400.
Zavala-Castro JE, Dzul-Rosado KR, Peniche-Lara G, Tello-Martín R, Zavala-Velázquez JE. Isolation of Rickettsia typhi from Human, México. Emerg Infect Dis. 2014;20:1411-2. http://dx.doi.org/10.3201/eid2008.130095.
Peniche-Lara G, Dzul-Rosado K, Pérez-Osorio C, Zavala-Castro J. Rickettsia typhi in rodents and R. felis in fleas in Yucatán, as a possible causal agent of undefined febrile cases. Rev Inst Trop Sao Paulo. 2015;57:129-32. http://dx.doi.org/10.1590/S0036-46652015000200005.
Instituto Nacional de Estadística y Geografía. Recursos naturales. Fecha de consulta: 3 de mayo de 2015. Disponible en: http://www.inegi.org.mx/geo/contenidos/recnat/default.aspx.
Choi YJ, Jang WJ, Ryu JS, Lee SH, Park KH, Paik HS, et al. Spotted fever group and typhus group rickettsioses in humans, South Korea. Emerg Infect Dis. 2005;11:237-44.
Webb L, Carl M, Malloy DC, Dasch GA, Azad AF. Detection of murine typhus in fleas by using the polimerase chain reaction. J Clin Microb. 1990;28:530-4.
Schriefer ME, Sacci JB Jr, Dumler JS, Bullen MG, Azad AF. Identification of a novel rickettsial infection in a patient diagnosed with murine typhus. J Clin Microbiol.1994;32: 949-54.
Peniche-Lara G, Zavala-Velázquez J, Dzul-Rosado K, Walker DH, Zavala-Castro JE. Simple method to differentiate among Rickettsia species. J Mol Microbiol Biotechnol. 2013;23:203-8. http://dx.doi.org/10.1159/000348298.
Hii SF, Kopp SR, Abdad MY, Thompson MF, O´Leary CA, Rees RL, et al. Molecular evidence supports the role of dogs as potential reservoirs for Rickettsia felis. Vector Borne Zoonotic Dis. 2011;11:1007-12. http://dx.doi.org/10.1089/vbz.2010.0270.
Kamani J, Baneth G, Mumcuoglu KY, Waziri NE, Eyal O, Guthmann Y, et al. Molecular detection and characteriza-tion of tick-borne pathogens in dogs and ticks from Nigeria. PLos Negl Trop Dis. 2013;7:e2108. http://dx.doi.org/10.1371/journal.pntd.0002108.
Barrett A, Little SE, Shaw E. "Rickettsia amblyommii" and R. montanensis infection in dogs following natural exposure to ticks. Vector Borne Zoonotic Dis. 2014;14:20-5. http://dx.doi.org/10.1089/vbz.2013.1325.
Solano-Gallego L, Caprì A, Pennisi MG, Caldin M, Furlanello T, Trotta M. Acute febrile illness is associated whit Rickettsia spp. infection in dogs. Parasit Vectors. 2015;10:216. http://dx.doi.org/10.1186/s13071-015-0824-3.
Huxsoll DL, Shirai A, Robinson DM, Yap LF, Lim BL. Presence of antibodies to scrub typhus and murine typhus in dogs from Selangor, Peninsular Malaysia. Southeast Asian J Trop Med Public Health. 1977;8:232-5.
Soliman AK, Botros BA, Ksiazek TG, Hoogstraal H, Helmy I, Morrill JC. Seroprevalence of Rickettsia typhi and Rickettsia conorii infection among rodents and dogs in Egypt. J Trop Med Hyg. 1989;92:345-9.
Bacellar F, Dawson JE, Silveira CA, Filipe AR. Antibodies against Rickettsiaceae in dogs of Seúbal, Portugal. Cent Eur J Public Health. 1995;3:100-2.
Lledó L, Gegúndez MI, Serrano JL, Saz JV, Beltrán M. A sero-epidemiological study of Rickettsia typhi infection in dogs from Soria province, central Spain. Ann Trop Med Parsitol. 2003;97:861-4.
Nogueras MM, Pons I, Ortuño A, Segura F. Seroprevalence of Rickettsia typhi and Rickettsia felis in dogs from north-eastern Spain. Clin Microbiol Infect. 2009;15:237-8. http://dx.doi.org/10.1111/j.1469-0691.2008.02156.x.
Nanayakkara DM, Rajapakse RP, Wickramasinghe S, Kularatne SA. Serological evidence for exposure of dogs to Rickettsia conorii, Rickettsia typhi and Orientia tsutsugamushi in Sri Lanka. Vector Borne Zoonotic Dis. 2013;13:545-9. http://dx.doi.org/10.1089/vbz.2012.1049.
Espejo E, Alegre MD, Font B, Font A, Segura F, Bella F. Antibodies to Rickettsia conorii in dogs: Seasonal differences. Eur J Epidemiol. 1993;9:344-6.
Tomassone L, Conte V, Parrilla G, De Meneghi D. Rickettsia infection in dogs and Rickettsia parkeri in Amblyomma tigrinum ticks, Cochabamba Department, Bolivia. Vector Borne Zoonotic Dis. 2010;10:953-8. http://dx.doi.org/10.1089/vbz.2009.0126.
Breitschwerdt EB, Moncol DJ, Corbett WT, MacCormack JN, Burgdorfer W, Ford RB, et al. Antibodies to spotted fever-group Rickettsiae in dogs in North Carolina. Am J Vet Res. 1987 48:1436-40.
Nicholson WL, Allen KE, McQuiston JH, Breitschwerdt EB, Little SE. The increasing recognition of rickettsial pathogens in dogs and people. Trends Parasitol. 2010;26: 205-12. http://dx.doi.org/10.1016/j.pt.2010.01.007.
Pinter A, Horta MC, Pacheco RC, Moraes-Filho J, Labruna MB. Serosurvey of Rickettsia spp. in dogs and humans from an endemic area for Brazilian spotted fever in the State of São Paulo, Brazil. Cad Saúde Pública. 2008;24:247-52. http://dx.doi.org/10.1590/S0102-311X2008000200003.
Algunos artículos similares:
- José Alejandro Martínez-Ibarra, Jorge Alejandro Martínez-Grant, Miguel Roberto Verdugo-Cervantes, Rafael Bustos-Saldaña, Benjamín Nogueda-Torres, Vigilancia de la presencia de triatominos mediante gallineros en el sur de Jalisco, México , Biomédica: Vol. 30 Núm. 1 (2010)
- Gladys Acuña-González, Carlo E. Medina-Solís, Gerardo Maupomé, Mauricio Escoffie-Ramírez, Jesús Hernández-Romano, María de L. Márquez-Corona, Arturo J. Islas-Márquez, Juan J. Villalobos-Rodelo, Factores de riesgo hereditarios y socioeconómicos para labio o paladar hendido no asociados a un síndrome en México: estudio de casos y controles pareado , Biomédica: Vol. 31 Núm. 3 (2011)
- Juan José Villalobos Rodelo, Carlo Eduardo Medina Solís, Nelly Molina Frechero, Ana Alicia Vallejos Sánchez, América Patricia Pontigo Loyola, José Luis Espinoza Beltrán, Caries dental en escolares de 6 a 12 añios de edad en Navolato, Sinaloa, México: experiencia, prevalencia, gravedad y necesidades de tratamiento. , Biomédica: Vol. 26 Núm. 2 (2006)
- Eduardo Rodríguez-Noriega, Gerardo León-Garnica, Santiago Petersen-Morfín, Héctor Raúl Pérez-Gómez, Esteban González-Díaz, Rayo Morfín-Otero, La evolución de la resistencia bacteriana en México, 1973-2013 , Biomédica: Vol. 34 (2014): Abril, Suplemento 1, Resistencia bacteriana
- Zinnia J. Molina-Garza, Lucio Galaviz-Silva, Pediculus capitis en niños de escuelas de la zona urbana de Nuevo León, México: análisis de factores asociados , Biomédica: Vol. 37 Núm. 3 (2017)
- Eduardo Bustos-Vázquez, Julián Alfredo Fernández-Niño, Claudia Iveth Astudillo-Garcia, Autopercepción de la salud, presencia de comorbilidades y depresión en adultos mayores mexicanos: propuesta y validación de un marco conceptual simple , Biomédica: Vol. 37 Núm. Sup.1 (2017): Suplemento 1, Alteraciones del sistema nervioso
- Analilia Solís-Hernández, Roger Iván Rodríguez-Vivas, María Dolores Esteve–Gassent, Sandra Luz Villegas-Pérez, Prevalencia de Borrelia burgdorferi sensu lato en roedores sinantrópicos de dos comunidades rurales de Yucatán, México , Biomédica: Vol. 36 (2016): Suplemento 1, Microbiología médica
- Claudio Alberto Dávila, Ana Melisa Pardo, Mortalidad por suicidios en Colombia y México: tendencias e impacto entre 2000 y 2013 , Biomédica: Vol. 36 Núm. 3 (2016)
- Lizbeth Díaz, Karen Covarrubias, Ángel Licón, Mixtli Astorga, Yaneth Moreno, José Alejandro Martínez, Parámetros biológicos de Meccus phyllosomus phyllosomus (Burmeister) 1835, de Triatoma recurva (Stål) 1868 (Hemiptera, Reduviidae) y de sus híbridos de laboratorio , Biomédica: Vol. 37 Núm. Sup. 2 (2017): Suplemento 2, Entomología médica, 2017
- Jesús Delgado-De la Mora, Jesús David Licona-Enríquez, Marcia Leyva-Gastélum, David Delgado-De la Mora, Adela Rascón-Alcantar, Gerardo Álvarez-Hernández, Una serie de casos fatales de fiebre manchada de las Montañas Rocosas en Sonora, México , Biomédica: Vol. 38 Núm. 1 (2018)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























