Inhibición parcial de dos genes que codifican para proteínas del empalmosoma en Giardia intestinalis
Resumen
Introducción. Giardia intestinalis es un organismo tempranamente divergente en el que recientemente se demostró la presencia de intrones. La maquinaria responsable de la remoción de intrones en organismos eucariotas superiores es el empalmosoma, el cual está conformado por cinco ribonucleoproteínas, cada una de las cuales tiene un ARN pequeño nuclear, un set de siete proteínas Sm (B, D1, D2, D3, E, F y G) y varias proteínas específicas. En G. intestinalis se han identificado los genes de algunas proteínas del empalmosoma por bioinformática. Aunque se asume que este es el responsable del empalme en el parásito, su caracterización bioquímica no se ha hecho.
Objetivo. Inhibir dos genes que codifican para proteínas del empalmosoma de G. intestinalis con el fin de determinar si esta inhibición afecta el crecimiento o el enquistamiento del parásito.
Materiales y métodos. En un vector específico para G. intestinalis se clonaron secuencias antisentido de los genes que codifican para las proteínas SmB y SmD3 del empalmosoma del parásito. Posteriormente, se transfectó G. intestinalis con los vectores recombinantes y se seleccionaron aquellos parásitos que lo incorporaron. Se confirmó la disminución del mensajero mediante reacción en cadena de la polimerasa (PCR) en tiempo real, y se evaluaron el crecimiento y el enquistamiento en parásitos silvestres y transfectados.
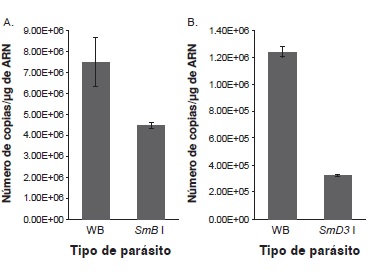
Resultados. Se observó una disminución de 40 y 70 % en el ARNm de SmB y SmD3, respectivamente. El crecimiento y el enquistamiento no se vieron afectados en estos parásitos.
Conclusión. La disminución de SmB y SmD3 no afectó al parásito, lo que indica que el empalmosoma sigue siendo funcional, o que el empalme no es una función vital del parásito.
Descargas
Referencias bibliográficas
Ankarklev J, Jerlström-Hultqvist J, Ringqvist E, Troell K, Svärd SG. Behind the smile: Cell biology and disease mechanisms of Giardia species. Nat Rev Microbiol. 2010;8:413-22. http://dx.doi.org/10.1038/nrmicro2317.
Painter JE, Gargano JW, Collier SA, Yoder JS, Centers for Disease Control and Prevention. Giardiasis surveillance – United States , 2011-2012. MMWR. 2015;64(Suppl):15-25.
Esch KJ, Petersen CA. Transmission and epidemiology of zoonotic protozoal diseases of companion animals. Clin Microbiol Rev. 2013;26:58-85. http://dx.doi.org/10.1128/CMR.00067-12.
Lujan HD, Mowatt MR, Byrd LG, Nash TE. Cholesterol starvation induces differentiation of the intestinal parasite Giardia lamblia. Proc Natl Acad Sci. 1996;93:7628-33. http://dx.doi.org/10.1073/pnas.93.15.7628.
Sogin M, Gunderson J, Elwood H, Alonso R, Peattie D. Phylogenetic meaning of the kingdom concept: An unusual ribosomal RNA from Giardia lamblia. Science. 1989;243:75-7. http://dx.doi.org/10.1126/science.2911720.
Best AA. Evolution of eukaryotic transcription: Insights from the genome of Giardia lamblia. Genome Res. 2004; 14:1537-47. http://dx.doi.org/10.1101/gr.2256604.
Morrison HG, McArthur AG, Gillin FD, Aley SB, Adam RD, Olsen GJ, et al. Genomic minimalism in the early diverging intestinal parasite Giardia lamblia. Science. 2007;317:1921-6. http://dx.doi.org/10.1126/science.1143837.
Nixon JE, Wang A, Morrison HG, McArthur AG, Sogin ML, Loftus BJ, et al. A spliceosomal intron in Giardia lamblia. Proc Natl Acad Sci USA. 2002;99:3701-5. http://dx.doi.org/10.1073/pnas.042700299.
Russell AG, Shutt TE, Watkins RF, Gray MW. An ancient spliceosomal intron in the ribosomal protein L7a gene (Rpl7a) of Giardia lamblia. BMC Evol Biol. 2005;5:45. http://dx.doi.org/10.1186/1471-2148-5-45.
Roy SW, Hudson AJ, Joseph J, Yee J, Russell AG. Numerous fragmented spliceosomal introns, AT-AC splicing, and an unusual dynein gene expression pathway in Giardia lamblia. Mol Biol Evol. 2012;29:43-9. http://dx.doi.org/10.1093/molbev/msr063.
Franzén O, Jerlström-Hultqvist J, Einarsson E, Ankarklev J, Ferella M, Andersson B, et al. Transcriptome profiling of Giardia intestinalis using strand-specific RNA-Seq. PLoS Comput Biol. 2013;9:e1003000. http://dx.doi.org/10.1371/journal.pcbi.1003000.
Kamikawa R, Inagaki Y, Hashimoto T. Secondary loss of a cis-spliced intron during the divergence of Giardia intestinalis assemblages. BMC Res Notes. 2014;7:413. http://dx.doi.org/10.1186/1756-0500-7-413.
Kamikawa R, Inagaki Y, Tokoro M, Roger AJ, Hashimoto T. Split introns in the genome of Giardia intestinalis are excised by spliceosome-mediated trans-splicing. Curr Biol. 2011;21:311-5. http://dx.doi.org/10.1016/j.cub.2011.01.025.
Nageshan RK, Roy N, Hehl AB, Tatu U. Post-transcriptional repair of a split heat shock protein 90 gene by mRNA trans-splicing. J Biol Chem. 2011;286:7116-22. http://dx.doi.org/10.1074/jbc.C110.208389.
Kambach C, Walke S, Young R, Avis JM, de la Fortelle E, Raker VA, et al. Crystal structures of two SM protein complexes and their implications for the assembly of the spliceosomal snRNPs. Cell. 1999;96:375-87. http://dx.doi.org/10.1016/S0092-8674(00)80550-4.
Raker VA, Plessel G, Lührmann R. The snRNP core assembly pathway: Identification of stable core protein heteromeric complexes and an snRNP subcore particle in vitro. EMBO J. 1996;15:2256-69.
Collins L, Penny D. Complex spliceosomal organization ancestral to extant eukaryotes. Mol Biol Evol. 2005;22: 1053-66. http://dx.doi.org/10.1093/molbev/msi091.
Keister DB. Axenic culture of Giardia lamblia in TYI-S-33 medium supplemented with bile. Trans R Soc Trop Med Hyg. 1983;77:487-8. http://dx.doi.org/10.1016/0035-9203(83)90120-7.
Kane AV, Ward HD, Keusch GT, Pereira ME. In vitro encystation of Giardia lamblia: Large-scale production of in vitro cysts and strain and clone differences in encystation efficiency. J Parasitol. 1991;77:974. http://dx.doi.org/10.2307/3282752.
Niño CA, Prucca CG, Chaparro J, Luján HD, Wasserman M. The ubiquitin-activating enzyme (E1) of the early-branching eukaryote Giardia intestinalis shows unusual proteolytic modifications and play important roles during encystation. Acta Trop. 2012;123:39-46. http://dx.doi.org/10.1016/j.actatropica.2012.03.012.
Teodorovic S, Walls CD, Elmendorf HG. Bidirectional transcription is an inherent feature of Giardia lamblia promoters and contributes to an abundance of sterile antisense transcripts throughout the genome. Nucleic Acids Res. 2007;35:2544-53. http://dx.doi.org/10.1093/nar/gkm105.
Prucca CG, Slavin I, Quiroga R, Elías E V, Rivero FD, Saura A, et al. Antigenic variation in Giardia lamblia is regulated by RNA interference. Nature. 2008;456:750-4. http://dx.doi.org/10.1038/nature07585.
Alvarado ME, Wasserman M. Calmodulin expression during Giardia intestinalis differentiation and identification of calmodulin-binding proteins during the trophozoite stage. Parasitol Res. 2012;110:1371-80. http://dx.doi.org/10.1007/s00436-011-2637-4.
Elmendorf HG. The abundance of sterile transcripts in Giardia lamblia. Nucleic Acids Res. 2001;29:4674-83. http://dx.doi.org/10.1093/nar/29.22.4674.
Wan L, Battle DJ, Yong J, Gubitz AK, Kolb SJ, Wang J, et al. The survival of motor neurons protein determines the capacity for snRNP assembly: Biochemical deficiency in spinal muscular atrophy. Mol Cell Biol. 2005;25:5543-51. http://dx.doi.org/10.1128/MCB.25.13.5543-5551.2005.
Algunos artículos similares:
- Carlos Alberto Niño, Moisés Wasserman, Síntesis de las enzimas de piruvato, oxidorreductasa de ferredoxina y deshidrogenasa E de alcohol durante el desenquistamiento (excystacion) de Giardia intestinalis , Biomédica: Vol. 30 Núm. 1 (2010)
- Zaava Ravid, Sofía Duque, Adriana Arévalo, Rubén Santiago Nicholls, Moisés Wasserman, Diversidad genética de poblaciones de Giardia intestinalis en Colombia , Biomédica: Vol. 27 Núm. 1 (2007)
- Paula C. Hernández, María Leonor Caldas, Moisés Wasserman, Enquistación in vitro de Giardia lamblia: análisis por electroforesis bidimensional de proteínas expresadas diferencialmente. , Biomédica: Vol. 22 Núm. 3 (2002)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























