Anticuerpos policlonales contra la proteína recombinante NS3 del virus del dengue
Resumen
Introducción. El dengue es una enfermedad causada por uno de los cuatro serotipos del virus del dengue (DENV) y es endémica en, aproximadamente, 130 países. Su incidencia ha aumentado notablemente en las últimas décadas, así como la frecuencia y la magnitud de los brotes. A pesar de los esfuerzos, no existen tratamientos profilácticos ni terapéuticos contra la enfermedad y, en ese contexto, el estudio de los procesos que gobiernan el ciclo de infección del DENV es esencial para
desarrollar vacunas o terapias antivirales. Una de las moléculas del DENV más prometedoras es la proteína no estructural 3 (NS3), la cual es indispensable para la replicación viral y es uno de los principales blancos inmunológicos durante la infección.
Objetivo. Producir anticuerpos policlonales para contribuir a los futuros estudios sobre las interacciones entre la proteína NS3 y otras proteínas celulares.
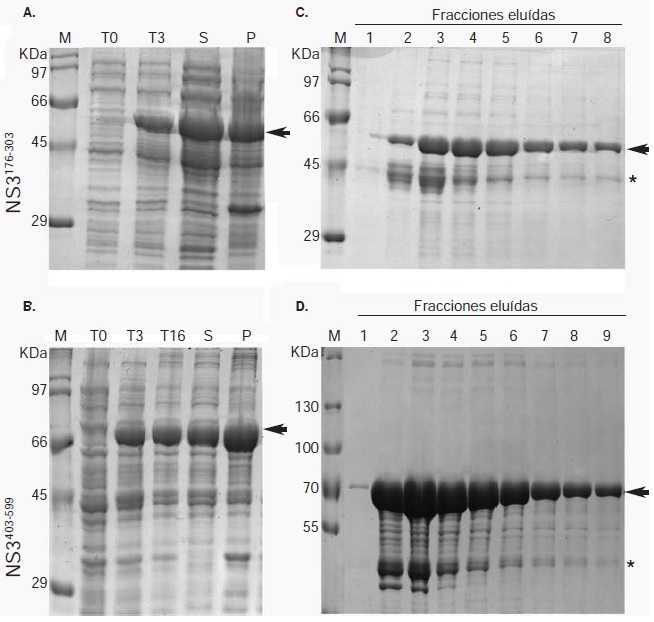
Materiales y métodos. Se expresaron dos proteínas recombinantes del dominio helicasa de NS3 del DENV de serotipo 2, las cuales se emplearon para inmunizar ratas y producir anticuerpos policlonales.
Resultados. Los anticuerpos producidos fueron útiles en ensayos de Western blot e inmunofluorescencia y se reportó por primera vez un anticuerpo policlonal anti-NS3 que permitió la inmunoprecipitación de la proteína viral y la detecta con Western blot sin necesidad de inducir sobreexpresión de NS3 o de usar extractos de células marcados metabólicamente con radioisótopos.
Conclusión. Las proteínas recombinantes expresadas y los anticuerpos producidos constituyen herramientas valiosas para estudiar procesos infecciosos del DENV que involucren a la proteína NS3 y evaluar pruebas dirigidas a interferir las funciones de esta proteína.
Descargas
Referencias bibliográficas
Bhatt S, Gething PW, Brady OJ, Messina JP, Farlow AW, Moyes CL, et al. The global distribution and burden of dengue. Nature. 2013;496:504-7. http://dx.doi.org/10.1038/nature12060
Chambers TJ, Hahn CS, Galler R, Rice CM. Flavivirus genome organization, expression, and replication. Annu Rev Microbiol. 1990;44:649-88. http://dx.doi.org/10.1146/
annurev.mi.44.100190.003245
Velandia ML, Castellanos JE. Virus del dengue: estructura y ciclo viral. Infectio. 2011;15:33-43. http://dx.doi.org/10.1016/S0123-9392(11)70074-1
Falgout B, Pethel M, Zhang YM, Lai CJ. Both nonstructural proteins NS2B and NS3 are required for the proteolytic processing of dengue virus nonstructural proteins. J Virol. 1991;65:2467-75.
Li H, Clum S, You S, Ebner KE, Padmanabhan R. The serine protease and RNA-stimulated nucleoside triphosphatase and RNA helicase functional domains of dengue virus type 2 NS3 converge within a region of 20 amino acids. J Virol. 1999;73:3108-16.
Bartelma G, Padmanabhan R. Expression, purification, and characterization of the RNA 5′-triphosphatase activity of dengue virus type 2 nonstructural protein 3. Virology. 2002;299:122-32. http://dx.doi.org/10.1006/viro.2002.1504
Duangchinda T, Dejnirattisai W, Vasanawathana S, Limpitikul W, Tangthawornchaikul N, Malasit P, et al. Immunodominant T-cell responses to dengue virus NS3 are associated with DHF. Proc Natl Acad Sci USA. 2010;107:16922-27. http://dx.doi.org/10.1073/pnas.1010867107
Rivino L, Kumaran EA, Jovanovic V, Nadua K, Teo EW, Pang SW, et al. Differential targeting of viral components by CD4+ versus CD8+ T lymphocytes in dengue infection. J Virol. 2012;87:2693-706. http://dx.doi.org/10.1128/JVI.02675-12
Chien LJ, Liao TL, Shu PY, Huang JH, Gubler DJ, Chang GJ. Development of real-time reverse transcriptase PCR assays to detect and serotype dengue viruses. J Clin Microbiol. 2006;44:1295-304. http://dx.doi.org/10.1128/JCM.44.4.1295-1304.2006
Costa SM, Yorio AP, Gonҫalves AJ, Vidale MM, Costa EC, Mohana-Borges R, et al. Induction of a protective response in mice by the dengue virus NS3 protein using DNA vaccines. PloSOne. 2011;6:e25685. http://dx.doi.org/10.1371/journal.pone.0025685
Smith DE, Fisher PA. Identification, developmental regulation, and response to heat shock of two antigenically related forms of a major nuclear envelope protein in Drosophila embryos: Application of an improved method for affinity purification of antibodies using polypeptides immobilized on nitrocellulose blots. J Cell Biol. 1984;99:20-8. http://dx.doi.org/10.1083/jcb.99.1.20
Zou J, Wang QY, Xie X, Lu S, Yau YH, Yuan Z, et al. Mapping the interactions between the NS4B and NS3 proteins of dengue virus. J Virol. 2015;89:3471-83. http://dx.doi.org/10.1128/JVI.03454-14
Mackenzie JM, Khromykh AA, Jones MK, Westaway EG. Subcellular localization and some biochemical properties of the flavivirus Kunjin nonstructural proteins NS2A and
NS4A. Virology. 1998;245:203-15. http://dx.doi.org/10.1006/viro.1998.9156
Kapoor M, Zhang L, Ramachandra M, Kusukawa J, Ebner KE, Padmanabhan R. Association between NS3 and NS5 proteins of dengue virus type 2 in the putative RNA replicase is linked to differential phosphorylation of NS5. J Biol Chem. 1995;270:19100-6. http://dx.doi.org/10.1074/jbc.270.32.19100
Chua JJ, Ng MM, Chow VT. The non-structural 3 (NS3) protein of dengue virus type 2 interacts with human nuclear receptor binding protein and is associated with alterations in membrane structure. Virus Res. 2004;102:151-63. http://dx.doi.org/10.1016/j.virusres.2004.01.025
Heaton NS, Perera R, Berger KL, Khadka S, Lacount DJ, Kuhn R J, et al. Dengue virus nonstructural protein 3 redistributes fatty acid synthase to sites of viral replication and increases cellular fatty acid synthesis. Proc Natl Acad Sci USA. 2010;107:17345-50. http://dx.doi.org/10.1073/pnas.1010811107
Arias CF, Preugschat F, Strauss JH. Dengue 2 virus NS2B and NS3 form a stable complex that can cleave NS3 within the helicase domain. Virology. 1993;193:888-99. http://dx.doi.org/10.1006/viro.1993.1198
Teo KF, Wright PJ. Internal proteolysis of the NS3 protein specified by dengue virus 2. J Gen Virol. 1997;78:337-41. http://dx.doi.org/10.1099/0022-1317-78-2-337
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























