Detección de Leishmania (V) guyanensis en ejemplares de Rhipicephalus (Boophilus) microplus (Acari: Ixodidae) recolectados en pecaríes de collar (Pecari tajacu)
Resumen
Introducción. En estudios previos se detectó la presencia de Leishmania infantum en Rhipicephalus sanguineus, lo cual planteaba la posibilidad de que R. sanguineus transmitiera la leishmaniasis a una variedad de huéspedes.
Objetivo. Identificar Leishmania (Viannia) spp. en garrapatas recolectadas en animales silvestres de una zona endémica para leishmaniasis.
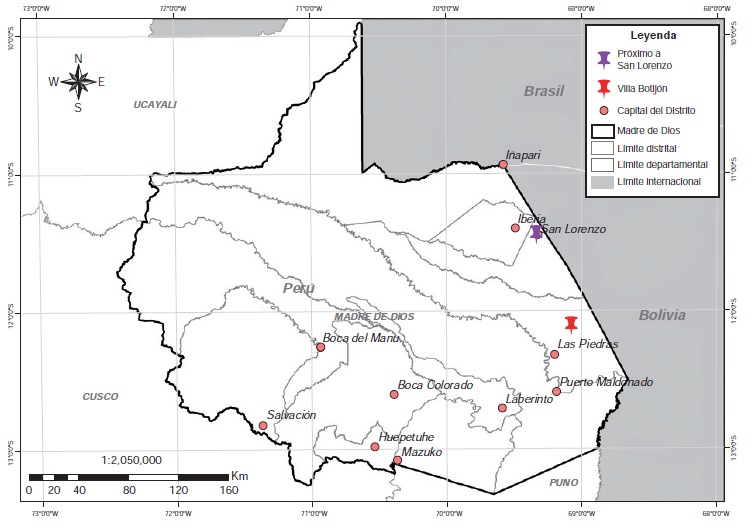
Materiales y métodos. Se hicieron 81 extracciones individuales de ADN en las garrapatas recogidas de tres tapires o dantas (Tapirus terrestres) y tres pecaríes de collar (Pecari tajacu) cazados en Madre de Dios, Perú. Las garrapatas recolectadas se identificaron taxonómicamente y se prepararon para la identificación del cinetoblasto (kDNA) de Leishmania (Viannia) spp. mediante reacción en cadena de la polimerasa (PCR), así como de la especie de Leishmania mediante PCR de fusión de alta resolución (High Resolution Melt, HRM).
Resultados. Se detectó el kDNA de Leishmania (V) spp. en tres garrapatas silvestres de R. (Boophilus) microplus, Canestrini, 1888, recolectadas en un pecarí de collar cazado en la selva de Madre de Dios. El análisis mediante HRM-PCR evidenció que una de las muestras positivas de kDNA tenía una curva compatible con L. (V) guyanensis.
Conclusión. Los resultados evidenciaron la presencia de ADN de L. (V) guyanensis en R. (Boophilus) microplus, probablemente adquirida después de picar al pecarí. Es importante hacer nuevos estudios para aclarar la participación de R. (Boophilus) microplus en la transmisión de la leishmaniasis.
Descargas
Referencias bibliográficas
Dantas-Torres F. Canine leishmaniosis in South America. Parasit Vectors. 2009;2(Suppl.1):1-8. https://doi.org/10.1186/
-3305-2-S1-S1
Solano-Gallego L, Rossi L, Scroccaro A, Montarsi F, Caldin M, Furlanello T, et al. Detection of Leishmania ticks removed from dogs living in endemic areas of canine leishmaniosis. Parasit Vectors. 2012;5:98. https://doi.org/10.1186/1756-3305-5-98
Colombo FA, Odorizzi RM, Laurenti MD, Galati EA, Canavez F, Pereira-Chioccola VL. Detection of Leishmania (Leishmania) infantum RNA in fleas and ticks collected from naturally infected dogs. Parasitol Res. 2011;2:267-74.
https://doi.org/10.1007/s00436-010-2247-6
Dantas-Torres F, Latrofa MS, Otranto D. Quantification of Leishmania infantum DNA in females, eggs, and larvae of Rhipicephalus sanguineus. Parasit Vectors. 2011;4:56. https://doi.org/10.1186/1756-3305-4-56
Dantas-Torres F. Ticks as vectors of Leishmania parasites. Trends Parasitol. 2011;27:155-9. https://doi.org/10.1016/j.pt.2010.12.006
Otranto D, Testini G, Dantas-Torres F, Latrofa MS, Vissotto de Paiva Diniz PP, de Caprariis D, et al. Diagnosis of canine vector-borne diseases in young dogs: A longitudinal study. J Clin Microbiol. 2010;48:3316-24. https://doi.org/10.1128/JCM.00379-10
Dantas-Torres F, Testini LV, de Paiva-Cavalcanti M, Figueredo LA, Stanneck D, Mencke N, et al. Detection of Leishmania infantum in Rhipicephalus sanguineus ticks from Brazil and Italy. Parasitol Res. 2010;106:857-60. https://doi.org/10.1007/s00436-010-1722-4
Sabogal S. Filogeografía y conservación genética del pecarí de collar, Pecari tajacu, en cuatro departamentos de Colombia (tesis). Bogotá: Universidad Nacional de Colombia; 2010.
Barros-Battesti D, Arzua M, Bechara H. Carrapatos de Importância Medico-Veterinaria da Região Neotropical: Um Guia Ilustrado para Identificação de Espécies. 10ma edição. Sao Paulo: Butantan Publicação; 2006. p. 223.
QIAGEN. Gentra®, Puregene® (QIAGEN Group), 2007-2010. Fecha de consulta: 9 de junio de 2017. Disponible en: https://
www.qiagen.com/us/shop/sample-technologies/dna/genomicdna/gentra-puregene-tissue-kit/#orderinginformation.
López M, Inga R, Cangalaya M, Echevarría J, Llanos-Cuentas A. Diagnosis the Leishmania using the polimerase chain reaction: A simplified procedure for field work. Am J Trop Med Hyg.1993;49:348-56. https://doi.org/10.4269/ajtmh.1993.49.348
Cabrera O, Munstermann L, Cárdenas R, Gutiérrez R, Ferro C. Definición de las condiciones de temperatura y almacenamiento adecuadas en la detección de ADN de Leishmania por PCR en flebotominos. Biomédica. 2002;22:296-302. https://doi.org/10.7705/biomedica.v22i3.1167
Labruna M, Romero M, Martins T, Tobler M, Ferrerira F.Ticks of the genus Amblyomma (Acari: Ixodidae) infesting tapirs (Tapirus terrestris) and peccaries (Tayassu pecari) in Perú. Syst Appl Acarol. 2010;15:109-12. https://doi.org/10.11158/saa.15.2.3
Otranto D, Dantas-Torres F. Canine and feline vector-borne diseases in Italy: Current situation and perspectives. Parasit Vectors. 2010;3:2. https://doi.org/10.1186/1756-3305-3-2
Rodríguez-Vivas R, Hodgkinson J, Trees A. Resistencia a los acaricidas en Rhipicephalus (Boophilus) microplus: situación actual y mecanismos de resistencia. Rev Mex Cienc Pecu. 2012;3:9-24.
Chen Z, Liu Q, Liu J, Xu B, Lv S, Xia S, et al. Tick-borne pathogens and associated co-infections in ticks collected
from domestic animals in central China. Parasit Vectors. 2014;7:237. https://doi.org/10.1186/1756-3305-7-237
Madder M, Adehan S, De Deken R, Adehan R, Lokossou R. New foci of Rhipicephalus microplus in West Africa. Exp Appl Acarol. 2012;56:385-90. https://doi.org/10.1007/s10493-012-9522-4
Guerrero F, Andreotti R, Bendele K, Cunha R, Miller R, Yeater K, et al. Rhipicephalus (Boophilus) microplus aquaporin as an effective vaccine antigen to protect against cattle tick infestations. Parasit Vectors. 2014;7:475. https://doi.org/1010.1186/s13071-014-0475-9
Goncalvez L, Filgueira K, Ahid S, Pereira J, Mendes do Vale A, Machado R, et al. Study on coinfecting vectorborne pathogens in dogs and ticks in Rio Grande do Norte, Brazil. Rev Bras Parasitol Vet. 2014;23:407-12. https://doi.org/10.1590/S1984-29612014071
Silva de Morais R, Goncalves-de-Albuquerquea S, Pessoa e Silva R, Lemos P, Gaudêncio da Silva K, Brandão-Filho S, et al. Detection and quantification of Leishmania braziliensis in ectoparasites from dogs. Vet Parasitol. 2013;196:506-8. https://doi.org/10.1016/j.vetpar.2013.03.026
Campos J, Costa F. Participation of ticks in the infectious cycle of canine visceral leishmaniasis, in Teresina, Piauí, Brazil. Rev Inst Med Trop Sao Paulo. 2014;56:297-300. https://doi.org/10.1590/S0036-46652014000400005
Ceccarelli M, Galluzzi L, Migliazzo A, Magnani M. Detection and characterization of Leishmania (Leishmania) and Leishmania (Viannia) by SYBR green-based real-time PCR and high resolution melt analysis targeting kinetoplast minicircle DNA. PLoS One. 2014;9:e88845. https://doi.org/10.1371/journal.pone.0088845
Lopes E, Geraldo C, Marcili A, Silva R, Keid L, Oliverira T, et al. Performance of conventional PCRs based on primers directed to nuclear and mitochondrial genes for the detection and identification of Leishmania spp. Rev Inst Med Trop Sao Paulo. 2016;58:41. https://doi.org/10.1590/S1678-9946201658041
Algunos artículos similares:
- Rafael José Vivero, Maria Angélica Contreras-Gutiérrez, Eduar Elías Bejarano, Análisis de la estructura primaria y secundaria del ARN de transferencia mitocondrial para serina en siete especies de Lutzomyia , Biomédica: Vol. 27 Núm. 3 (2007)
- Elsa Nieves, Neudo Buelvas, Maritza Rondón, Néstor González, Las glándulas salivales de dos flebotominos vectores de Leishmania: Lutzomyia migonei (França) y Lutzomyia ovallesi (Ortiz) (Diptera: Psychodidae) , Biomédica: Vol. 30 Núm. 3 (2010)
- Carlos Pérez, Yoanet Solías, Gerzaín Rodríguez, Leishmaniasis cutánea difusa en un paciente con sida , Biomédica: Vol. 26 Núm. 4 (2006)
- María Angélica Contreras, Rafael José Vivero, Eduar Elías Bejarano, Lina María Carrillo, Iván Darío Vélez, Nuevos registros de flebotomíneos (Diptera: Psychodidae) en el área de influencia del río Amoyá en Chaparral, Tolima , Biomédica: Vol. 32 Núm. 2 (2012)
- Luz Adriana Acosta, Karina Mondragon-Shem, Daniela Vergara, Andrés Velez-Mira, Horacio Cadena, Lina Maria Carrillo, Ampliación de la distribución de Lutzomyia longipalpis (Lutz & Neiva, 1912) (Diptera: Psychodidae) en el departamento de Caldas: potencial aumento del riesgo de leishmaniasis visceral , Biomédica: Vol. 33 Núm. 2 (2013)
- Héctor de Lima, José Carrero, Armando Rodríguez, Zoraya de Guglielmo, Noris Rodríguez, Trypanosomatidae de importancia en salud pública en animales silvestres y sinantrópicos en un area rural del municipio Tovar del estado Mérida, Venezuela. , Biomédica: Vol. 26 Núm. 1 (2006)
- Clemencia Ovalle-Bracho, Carolina Camargo, Yira Díaz-Toro, Marcela Parra-Muñoz, Tipificación molecular de Leishmania (Leishmania) amazonensis y especies del subgénero Viannia asociadas a la leishmaniasis cutánea y la mucosa en Colombia: un estudio de concordancia , Biomédica: Vol. 38 Núm. 1 (2018)
- María Angélica Contreras-Gutiérrez, Iván Darío Vélez, Charles Porter, Sandra Inés Uribe, Lista actualizada de flebotomíneos (Diptera: Psychodidae: Phlebotominae) de la región cafetera colombiana , Biomédica: Vol. 34 Núm. 3 (2014)
- Catalina Marceló, Olga Lucía Cabrera, Erika Santamaría, Indicadores de sensibilidad de una cepa experimental de Lutzomyia longipalpis (Diptera: Psychodidae) a tres insecticidas de uso en salud pública en Colombia , Biomédica: Vol. 34 Núm. 4 (2014)
- Emy Luz Sánchez, Gílmar Gabriel Santafé, Omar Leonardo Torres, Diana Lorena Muñoz, Sara María Robledo, Compuestos sintéticos del tipo de estirilquinolinas con actividades leishmanicida y citotóxica , Biomédica: Vol. 34 Núm. 4 (2014)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























