Polimorfismos de un solo nucleótido representativos para los alelos clásicos del antígeno leucocitario humano en familias antioqueñas con diabetes mellitus tipo 1
Resumen
Introducción. La región del antígeno leucocitario humano (Human Leukocyte Antigen, HLA) se ha asociado claramente con enfermedades autoinmunitarias, como la diabetes mellitus de tipo 1. Los polimorfismos representativos de un solo nucleótido (tag Single Nucleotide Polymorphism, tag SNP) constituyen una forma alternativa de evaluar los alelos clásicos del HLA. En la población europea se ha reportado un grupo de tag SNP para múltiples alelos clásicos relacionados con la predisposición o la resistencia frente a dicha enfermedad.
Objetivo. Validar la metodología basada en los tag SNP enfocada en la inferencia de alelos HLA clásicos, y evaluar su asociación con la diabetes mellitus de tipo 1 en una muestra de familias antioqueñas.
Materiales y métodos. Se estudió una muestra de 200 familias antioqueñas con uno a dos hijos afectados por diabetes mellitus de tipo 1. Se genotipificaron 13 SNP mediante el ARMS-PCR (Amplification Refractory Mutation System-Polymerase Chain Reaction) con cuatro iniciadores, o mediante la PCR-RFLP (PCR-Restriction Fragment Length Polymorphism). Además, se evaluó la validez de los tag SNP de 1.000 genomas reportados en europeos en una muestra de 60 individuos de la población colombiana de Medellín. Se hicieron las pruebas de desequilibrio de la transmisión, de desequilibrio de ligamiento y de equilibrio de Hardy-Weinberg.
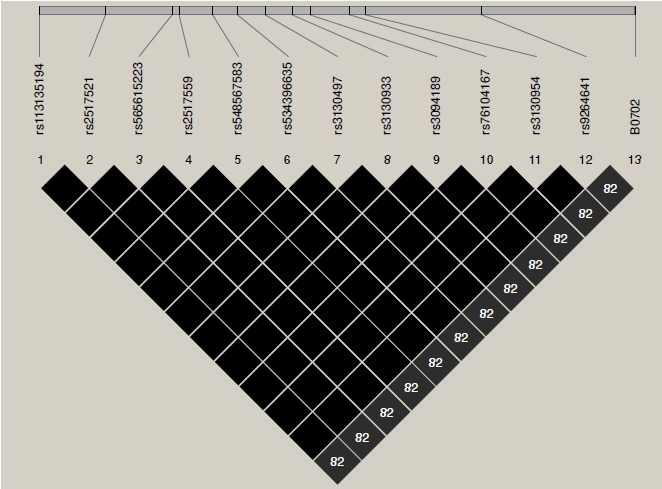
Resultados. En la población de estudio no se encontró suficiente desequilibrio de ligamiento entre los SNP y los alelos clásicos evaluados, por lo cual no fue posible inferir los alelos clásicos del HLA para el conjunto de familias con diabetes mellitus de tipo 1. El estudio de asociación evidenció que esta región aporta factores tanto de riesgo como de protección para el desarrollo de la enfermedad. Los tag SNP apropiados para la muestra de estudio se determinaron usando los SNP ubicados en la región HLA en la base de datos del 1000 Genomes Project en la mencionada población.
Conclusiones. Los patrones de desequilibrio de ligamiento en la población estudiada fueron diferentes a los reportados para la población europea. A pesar de esto, se encontró evidencia clara sobre el papel de la región HLA en el riesgo de padecer diabetes mellitus de tipo 1 en la población de estudio.
Descargas
Referencias bibliográficas
Kim MS, Polychronakos C. Immunogenetics of type 1 diabetes. Horm Res. 2005;64:180-8. https://doi.org/10.1159/000089190
Černá M. Genetics of autoimmune diabetes mellitus. Wien Med Wochenschr. 2008;158:2-12. https://doi.org/10.1007/s10354-007-0448-0
Concannon P, Rich SS, Nepom GT. Genetics of type 1A diabetes. N Engl J Med. 2009;360:1646-54. https://doi.org/10.1056/NEJMra0808284
Al-Mutairi HF, Mohsen AM, Al-Mazidi ZM. Genetics of type 1 diabetes mellitus. Kuwait Med J. 2007;39:107-15.
Sia C, Weinem M. The role of HLA class I gene variation in autoimmune diabetes. Rev Diabet Stud. 2005;2:97-109.https://doi.org/10.1900/RDS.2005.2.97
Noble JA, Valdés AM, Varney MD, Carlson JA, Moonsamy P, Fear AL, et al. HLA class I and genetic susceptibility to type 1 diabetes: Results from the Type 1 Diabetes Genetics Consortium. Diabetes. 2010;59:2972-9. https://doi.org/10.2337/db10-0699
Cruz-Tapias P, Pérez-Fernández OM, Rojas-Villarraga A, Rodríguez-Rodríguez A, Arango M-T, Anaya JM. Shared HLA class II in six autoimmune diseases in Latin America: A meta-analysis. Autoimmune Dis. 2012;2012:569728. https://doi.org/10.1155/2012/569728
Montoya F, Bedoya CI, Restrepo MC, Villegas A, Posada SC, García HI, et al. Determinación de marcadores genéticos en pacientes con diabetes tipo I y población sana. Acta Médica Colombiana. 1996;21:10-6.
de Bakker PI, McVean G, Sabeti PC, Miretti MM, Green T, Marchini J, et al. A high-resolution HLA and SNP haplotype map for disease association studies in the extended human MHC. Nat Genet. 2006;38:1166-72. https://doi.org/10.1038/ng1885
Halperin E, Kimmel G, Shamir R. Tag SNP selection in genotype data for maximizing SNP prediction accuracy. Bioinformatics. 2005;21(Suppl.1):i195-203. https://doi.org/10.1093/bioinformatics/bti1021
Barker JM, Triolo TM, Aly TA, Baschal EE, Babu SR, Kretowski A, et al. Two single nucleotide polymorphisms identify the highest-risk diabetes HLA genotype potential for rapid screening. Diabetes. 2008;57:3152-5. https://doi.org/10.2337/db08-0605
American Diabetes Association. Classification and diagnosis of diabetes. Diabetes Care. 2016;39(Supl.1):S13-22. https://doi.org/10.2337/dc16-er09
Ye S, Dhillon S, Ke X, Collins AR, Day IN. An efficient procedure for genotyping single nucleotide polymorphisms. Nucleic Acids Res. 2001;29:E88-8.
Vincze T, Posfai J, Roberts R. NEBcutter: A program to cleave DNA with restriction enzymes. Nucleic Acids Res. 2003;31:3688-91.
Durbin RM, Altshuler DL, Abecasis GR, Bentley DR, Chakravarti A, Clark AG, et al. A map of human genome variation from population-scale sequencing. Nature. 2010;467:1061-73. https://doi.org/10.1038/nature09534
Gourraud PA, Khankhanian P, Cereb N, Yang SY, Feolo M, Maiers M, et al. HLA diversity in the 1000 genomes dataset. PLoS One. 2014;9:e97282. https://doi.org/1010.
/journal.pone.0097282
Barrett JC, Fry B, Maller J, Daly MJ. Haploview: Analysis and visualization of LD and haplotype maps. Bioinformatics. 2005;21:263-5. https://doi.org/10.1093/bioinformatics/bth457
Purcell S, Neale B, Todd-Brown K, Thomas L, Ferreira MA, Bender D, et al. PLINK: A tool set for whole-genome association and population-based linkage analyses. Am J Hum Genet. 2007;81:559-75. https://doi.org/10.1086/519795
Spielman RS, Ewens WJ. The TDT and other family-based tests for linkage disequilibrium and association. Am J Hum Genet. 1996;59:983-9.
Dudbridge F. Likelihood-based association analysis for nuclear families and unrelated subjects with missing genotype data. Hum Hered. 2008;66:87-98. https://doi.org/10.1159/000119108
Li Q, Fallin MD, Louis TA, Lasseter VK, McGrath JA, Avramopoulos D, et al. Trio logic regression - detection of SNP-SNP interactions in case-parent trios. Genet Epidemiol. 2010;34:396-406. https://doi.org/10.1002/gepi.20488
Rodríguez A, Alfaro JM, Balthazar V, Pineda-Trujillo N. Association analysis of PTPN22, CTLA4 and IFIH1 genes with type 1 diabetes in Colombian families. J Diabetes. 2015;7:402-10. https://doi.org/10.1111/1753-0407.12192
Slatkin M. Linkage disequilibrium — understanding the evolutionary past and mapping the medical future. Nat Rev Genet. 2008;9:477-85. https://doi.org/10.1038/nrg2361
Bedoya G, Montoya P, García J, Soto I, Bourgeois S, Carvajal L, et al. Admixture dynamics in Hispanics: A shift in the nuclear genetic ancestry of a South American population isolate. Proc Natl Acad Sci USA. 2006;103:7234-9. https://doi.org/10.1073/pnas.0508716103
Gravel S, Zakharia F, Moreno-Estrada A, Byrnes JK, Muzzio M, Rodríguez-Flores JL, et al. Reconstructing Native American migrations from whole-genome and wholeexome data. PLoS Genet. 2013;9:e1004023. https://doi.org/10.1371/journal.pgen.1004023
Stephens JC, Schneider JA, Tanguay DA, Choi J, Acharya T, Stanley SE, et al. Haplotype variation and linkage disequilibrium in 313 human genes. Science. 2001;293:489-93. https://doi.org/10.1126/science.1059431
Federal Research Division Library of Congress. Colombia: A country study. 5th ed. Washington, D.C.; U.S. Government Printing Office Official Editions; 2010. p. 541.
Miretti MM, Walsh EC, Ke X, Delgado M, Griffiths M, Hunt S, et al. A high-resolution linkage-disequilibrium map of the human major histocompatibility complex and first generation of tag single-nucleotide polymorphisms. Am J Hum Genet. 2005;76:634-46. https://doi.org/10.1086/429393
Rani R, Sood A, Goswami R. Molecular basis of predisposition to develop type 1 diabetes mellitus in North Indians. Tissue Antigens. 2004;64:145-55. https://doi.org/10.1111/j.1399-0039.2004.00246.x
Aly TA, Ide A, Jahromi MM, Barker JM, Fernando MS, Babu SR, et al. Extreme genetic risk for type 1A diabetes. Proc Natl Acad Sci USA. 2006;103:14074-9. https://doi.org/10.1073/pnas.0606349103
Noble JA, Martin A, Valdés AM, Lane JA, Galgani A, Petrone A, et al. Type 1 diabetes risk for HLA-DR3 haplotypes depends on genotypic context: Association of DPB1 and HLA class I loci among DR3 and DR4 matched Italian patients and controls. Hum Immunol. 2008;69:291-300. https://doi.org/10.1016/j.humimm.2008.02.003
Mbunwe E, van der Auwera BJ, Weets I, van Crombrugge P, Crenier L, Coeckelberghs M, et al. In antibody-positive first-degree relatives of patients with type 1 diabetes, HLA-A*24 and HLA-B*18, but not HLA-B*39, are predictors of impending diabetes with distinct HLA-DQ interactions. Diabetologia. 2013;56:1964-70. https://doi.org/10.1007/s00125-013-2951-8
Algunos artículos similares:
- Angélica María Delgado-Vega, Javier Martín, Julio Granados, Juan Manuel Anaya, Epidemiología genética de la artritis reumatoide: ¿qué esperar de América Latina? , Biomédica: Vol. 26 Núm. 4 (2006)
- Gloria Garavito, Eduardo Egea, Luis Fang, Clara Malagón, Carlos Olmos, Luz González, Pilar Guarnizo, Gustavo Aroca, Guillermo López, Antonio Iglesias, Asociación de variantes polimorfas de los genes PTPN22, TNF y VDR en niños con nefritis lúpica: un estudio de tríos en familias colombianas , Biomédica: Vol. 37 Núm. 2 (2017)
- María Isabel García, Camila Céspedes, Paola Durán , Catalina Forero, Mauricio Coll , Evaluación de la calidad de vida en niños y adolescentes con diabetes de tipo 1 en dos instituciones de salud, Bogotá, D. C., Colombia , Biomédica: Vol. 43 Núm. 1 (2023)
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |

























